Ci sono scoperte che cambiano il modo di valutare il bilancio del carbonio e che danno indicazioni per certi aspetti rivoluzionarie sul ruolo svolto dalle foreste e su come una foresta svolga il proprio ruolo di deposito del carbonio.
Su Nature di una decina di anni fa, N.L. Stephenson e altri 37 colleghi, dopo aver esaminato centinaia di migliaia di alberi di oltre 400 specie diverse in tutto il mondo hanno concluso che non è vero che gli alberi anziani sono meno importanti di quelli giovani nel ciclo del carbonio; è vero che con l’età la loro efficienza diminuisce ma i grandi alberi, i più antichi della foresta, rimediano a questo grazie alla amplissima superficie fogliare; in pratica nella maggior parte delle specie la velocità di crescita della massa dell’albero aumenta con le sue dimensioni.
Come conseguenza di ciò i grandi vecchi alberi non sono semplicemente riserve di carbonio che invecchiano, ma essi fissano attivamente grandi quantità di carbonio se paragonati ad alberi più piccoli; in casi estremi un singolo albero molto grande può aggiungere alla foresta in un solo anno la stessa quantità di carbonio di quella contenuta in un intero albero di medie dimensioni.
Questo cambia la nostra visuale della foresta e della vita vegetale; è vero che gli alberi invecchiano, ma al contrario di noi il loro contributo metabolico (nel loro caso l’accumulazione del carbonio) aumenta con l’età; molti lavori precedenti si erano concentrati sulla vita della foresta e sulla sua evoluzione complessiva, ma avevano trascurato questo elemento specifico. L’abbattimento di un albero vecchio non può essere giustificato da un supposto minore contributo alla foresta come tale; gli alberi anziani, come tutti gli organismi, possono ammalarsi e/o morire, ma se vivono il loro contributo aumenta e non diminuisce.
Claudio Della Volpe
Qui di seguito la traduzione dell’articolo pubblicato su Nature il 15.01.2014.
![]()
Il tasso di accumulo di carbonio negli alberi aumenta continuamente con le dimensioni dell'albero
N.L. Stephenson, et al.
Abstract
Le foreste sono componenti importanti del ciclo globale del carbonio e forniscono un feedback sostanziale alle concentrazioni atmosferiche di gas serra1. La nostra capacità di comprendere e prevedere i cambiamenti nel ciclo del carbonio delle foreste, in particolare la produttività primaria netta e l'immagazzinamento del carbonio, si basa sempre più su modelli che rappresentano i processi biologici su diverse scale di organizzazione biologica, dalle foglie degli alberi ai popolamenti forestali2,3. Tuttavia, nonostante i progressi nella comprensione della produttività a livello delle foglie e dei popolamenti, non esiste un consenso sulla natura della produttività su scala di singolo albero4-7, in parte perché manca un'ampia valutazione empirica del fatto che i tassi di crescita assoluta della massa arborea (e quindi l'accumulo di carbonio) diminuiscano, rimangano costanti o aumentino, all'aumentare delle dimensioni e dell'età degli alberi.
Qui presentiamo un'analisi globale di 403 specie arboree tropicali e temperate, dimostrando che per la maggior parte delle specie, il tasso di crescita della massa aumenta continuamente con le dimensioni dell'albero. Pertanto, gli alberi grandi e vecchi non agiscono semplicemente come serbatoi di carbonio senescenti, ma fissano attivamente grandi quantità di carbonio rispetto agli alberi più piccoli; all'estremo, in un anno, un singolo grande albero può aggiungere alla foresta la stessa quantità di carbonio contenuta in un intero albero di medie dimensioni. Gli apparenti paradossi dell'aumento del tasso di accumulo con la crescita delle loro dimensioni, nonostante il calo della produttività a livello di fogliame8-10 e di popolamento10, possono essere spiegati, rispettivamente, dall'aumento dell'area fogliare totale di un albero che supera il calo della produttività per unità di area fogliare e, tra gli altri fattori, dalla riduzione della densità di popolazione legata all'età. I nostri risultati risolvono ipotesi contrastanti sulla natura della crescita degli alberi, forniscono informazioni sulla comprensione e sulla modellazione delle dinamiche del carbonio nelle foreste e hanno ulteriori implicazioni sulle teorie dell'allocazione delle risorse11 e la senescenza delle piante12.
Un'ipotesi ampiamente condivisa è che, dopo un periodo iniziale di aumento della crescita, il tasso di crescita della massa dei singoli alberi diminuisca con l'aumentare delle dimensioni4,5,13-16. Sebbene i risultati di alcuni studi su singole specie siano stati coerenti con questa ipotesi15, la maggior parte delle prove citate a sostegno del declino della crescita non si basa su misurazioni della crescita della massa dei singoli alberi. Al contrario, gran parte delle prove citate documentano il ben noto declino legato all'età della produttività primaria netta (di seguito “produttività”) dei popolamenti forestali di età uniforme10 (in cui gli alberi hanno tutti un'età simile) o il declino legato alle dimensioni del tasso di incremento di massa per unità di area fogliare (o unità di massa fogliare)8-10, con l'implicito presupposto che i declini su tale scala debbano applicarsi anche a livello del singolo albero.
Anche la diminuzione della crescita degli alberi è talvolta dedotta dalla teoria del ciclo vitale [life-history], come un corollario necessario dell'aumento delle risorse destinate alla riproduzione 11,16. D'altra parte, la teoria della scalarità metabolica prevede che il tasso di crescita della massa aumenti continuamente con le dimensioni dell'albero 6, e questa previsione ha ricevuto anche un supporto empirico da alcuni studi specifici sul campo6,7. Ci troviamo quindi di fronte a due generalizzazioni contrastanti sulla natura fondamentale della crescita degli alberi, ma manca una valutazione globale che ci permetta di distinguerle chiaramente. Per colmare questa lacuna, abbiamo condotto un'analisi globale in cui abbiamo stimato direttamente i tassi di crescita della massa, con misurazioni ripetute su 673.046 alberi appartenenti a 403 specie tropicali, subtropicali e temperate, che coprono tutti i continenti boscosi. Il tasso di crescita degli alberi è stato modellato come una funzione logaritmica della massa dell'albero, utilizzando la "regressione segmentata", in cui la variabile indipendente è stata suddivisa in un numero di intervalli da uno a quattro. Sono stati applicati segmenti di linea tra i diversi intervalli (Fig. 1).
Figura 1 | Esempio di adattamento del modello per i tassi di crescita della massa degli alberi.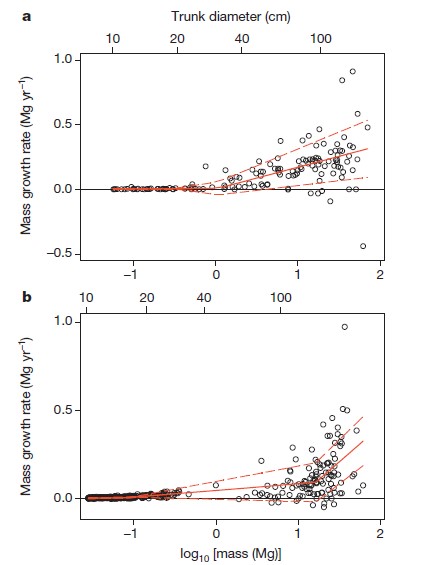
Le specie rappresentate sono le angiosperme (Lecomtedoxa klaineana, Camerun, 142 alberi) (a) e le gimnosperme (Picea sitchensis, USA, 409 alberi) (b), del nostro insieme di dati che riguardavano gli alberi più massicci (definiti come quelli con la maggiore massa secca cumulativa in superficie nei cinque alberi più massicci). Ogni punto rappresenta un singolo albero; le linee rosse continue rappresentano i migliori adattamenti selezionati dal nostro modello; le linee rosse tratteggiate indicano una deviazione standard intorno ai valori previsti.
In tutti i continenti, i tassi di crescita della massa arborea in superficie (e, quindi, i tassi di guadagno di carbonio) per la maggior parte delle specie sono aumentati in modo continuo con la massa dell'albero (dimensioni) (Fig. 2). Il tasso di incremento di massa è cresciuto con la massa dell'albero in ogni intervallo del modello per l'87% delle specie, ed è aumentato nell'intervallo che comprendeva gli alberi più grandi per il 97% delle specie; la maggior parte degli aumenti era statisticamente significativa (Tabella 1, Dati estesi Fig. 1 e Tabella supplementare 1).
Figura 2 | Tassi di crescita della massa arborea per le 403 specie arboree, per continente. 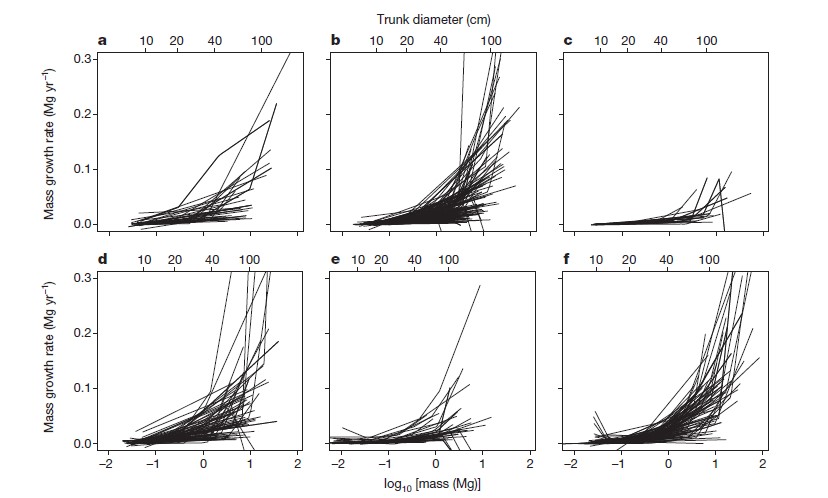
a, Africa (Camerun, Repubblica Democratica del Congo); b, Asia (Cina, Malesia, Taiwan, Tailandia); c, Australasia (Nuova Zelanda); d, America Centrale e Meridionale (Argentina, Colombia, Panama); e, Europa (Spagna); f, America Settentrionale (Stati Uniti). Il totale degli alberi, il numero delle specie e le percentuali con una crescita in aumento sono riportati nella Tabella 1. I diametri del tronco sono valori approssimativi di riferimento, basati sui diametri medi degli alberi di una determinata massa.
Tabella 1 | Dimensioni del campione e tendenze di crescita degli alberi per continente
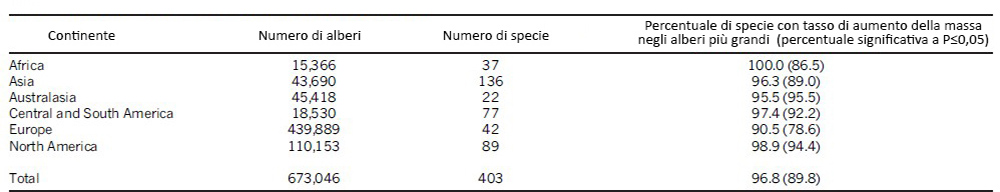
Gli alberi più grandi sono quelli dell'ultimo intervallo adattato dal modello. I Paesi sono elencati nella legenda dellaFig. 2.
Anche quando abbiamo ristretto la nostra analisi alle specie che raggiungevano le dimensioni più grandi (diametro massimo del tronco > 100 cm; 33% delle specie), il 94% aveva tassi di accrescimento della massa crescenti nell'intervallo che comprendeva gli alberi più grandi. Non sono stati riscontrati chiari schemi tassonomici o geografici tra il 3% delle specie con tassi di crescita in calo negli alberi più grandi, anche se il numero ridotto di queste specie (tredici) ne ostacola l'inferenza. Le specie in declino comprendevano sia angiosperme che gimnosperme in sette delle 76 famiglie del nostro studio; la maggior parte delle sette famiglie aveva solo una o due specie in declino e nessuna famiglia era dominata da specie in declino (Tabella supplementare 1).
Quando abbiamo messo in scala logaritmica il tasso di crescita della massa, in aggiunta alla massa degli alberi, i modelli risultanti erano generalmente lineari, come previsto dalla teoria dello "scaling metabolico" (o anche leggi allometriche)6(Dati estesi Fig. 2). Analogamente ai risultati della nostra analisi principale utilizzando la crescita non trasformata, delle 381 specie analizzate a scala logaritmica (vedi Metodi), il tasso di crescita su base logaritmica è aumentato nell’intervallo contenente gli alberi più grandi per il 96% delle specie.
In termini assoluti, gli alberi di 100 cm di diametro di tronco aggiungono, in genere, da 10 kg a 200 kg di massa secca fuori terra ogni anno (a seconda della specie), con una media di 103 kg all'anno. Si tratta di un tasso quasi triplo rispetto a quello degli alberi della stessa specie con un diametro di 50 cm, ed è la massa equivalente a un nuovo albero di 10-20 cm di diametro aggiunto alla foresta ogni anno. I nostri risultati indicano inoltre che la crescita straordinaria - recentemente riportata in uno studio intensivo di grandi Eucalyptus regnans e Sequoia sempervirens7 - che riguardava alcuni degli alberi singoli più imponenti del mondo, non è un fenomeno limitato a poche insolite specie. Piuttosto, la rapida crescita degli alberi giganti è la norma a livello globale, e può superare i 600 kg all'anno negli individui più grandi (Fig. 3).
Figura 3 | Tassi di crescita arborea rispetto a Eucalyptus regnans e Sequoia sempervirens.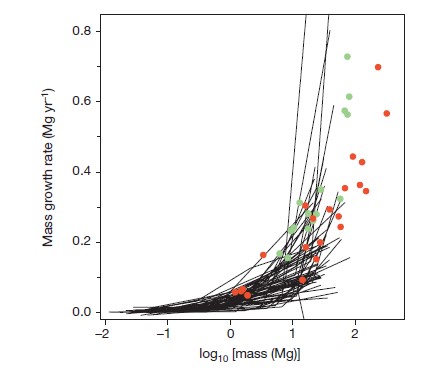
Per chiarezza, sono mostrate solo le 58 specie dell’insieme di dati con almeno un albero che supera i 20Mg (linee). I dati per E. regnans (punti verdi, 15 alberi) e S. sempervirens (punti rossi, 21 alberi) provengono da un approfondito studio che ha incluso alcuni degli alberi più imponenti della Terra7. Entrambi gli assi sono stati ampliati rispetto a quelli della Fig. 2.
Il nostro insieme di dati comprendeva foreste naturali e non gestite, in cui la crescita degli alberi più piccoli era probabilmente ridotta dalla competizione asimmetrica con gli alberi più grandi. Per esaminare gli effetti della competizione, abbiamo calcolato i tassi di crescita della massa per 41 specie nordamericane ed europee che avevano equazioni pubblicate sui tassi di crescita del diametro, in assenza di competizione. Abbiamo riscontrato che, anche in assenza di competizione, l'85% delle specie aveva tassi di crescita della massa che aumentavano in modo continuo con le dimensioni dell'albero (Dati estesi Fig. 3), con curve di crescita molto simili a quelle della Fig. 2. Pertanto, la nostra scoperta di un incremento crescente, non solo ha un'ampia generalità tra le specie, i continenti e i biomi forestali (tropicale, subtropicale e temperato), ma sembra essere valida indipendentemente dall'ambiente competitivo.
È importante notare che la nostra scoperta di una crescita in continuo aumento è compatibile con le due osservazioni più spesso citate come prova della diminuzione, piuttosto che dell'aumento, della crescita dei singoli alberi: con l'aumento delle dimensioni e dell'età degli alberi, la produttività di solito diminuisce sia a livello di organi (foglie) che di popolazioni di alberi (popolamenti forestali di età uniforme).
In primo luogo, sebbene l'efficienza della crescita (aumento della massa arborea per unità di superficie fogliare o massa fogliare) spesso diminuisca con l'aumentare delle dimensioni dell'albero8-10, le osservazioni empiriche e la teoria della scalarità metabolica indicano entrambe che, in media, la massa fogliare totale dell'albero aumenta con il quadrato del diametro del tronco17,18.
Un tipico albero, che avrà un aumento del diametro di 10 volte, avrà quindi un aumento della massa fogliare totale di circa 100 volte, e un aumento dell'area fogliare totale di 50-100 volte (a seconda dell’aumento della massa fogliare per unità di area fogliare19,20). I contemporanei cambiamenti nell'efficienza di crescita possono variare da un modesto aumento (come nei popolamenti in cui gli alberi piccoli sono soffocati da quelli grandi)21 a un calo fino a 10 volte22, con la maggior parte dei cambiamenti che si collocano nel mezzo8,9,19,22.
Da un lato, l'effetto netto di un aumento modesto (50 volte) dell'area fogliare, combinato con un'ampia diminuzione (10 volte) dell'efficienza di crescita, produrrebbe comunque un aumento di 5 volte del tasso di crescita della massa di un singolo albero; all'estremo opposto si otterrebbe un aumento di circa 100 volte. Il tasso di crescita medio, da noi calcolato, della massa degli alberi di 100 cm di diametro, è di 52 volte superiore rispetto a quello degli alberi di 10 cm di diametro. Pertanto, sebbene l'efficienza della crescita spesso diminuisca con l'aumentare delle dimensioni dell'albero, l'aumento dell'area fogliare totale di un albero è sufficiente a superare questo calo, e a far aumentare il tasso di accumulo di carbonio dell'intero albero.
In secondo luogo, i nostri risultati sono altrettanto compatibili con il ben noto calo della produttività su scala di popolamento forestale, legato all'età. Sebbene una rassegna dei meccanismi esuli dallo scopo di questo articolo10,23, diversi fattori (tra cui l'interazione tra il cambiamento dell'efficienza di crescita e le gerarchie di dominanza degli alberi24) possono contribuire al declino della produttività su scala di popolamento, sottolineando il fatto che l’aumento del tasso di crescita dei singoli alberi non si traduce automaticamente in un aumento della produttività del popolamento, poiché la mortalità degli alberi può determinare riduzioni in ordine di grandezza della densità della popolazione25-26. In altre parole, anche se i grandi alberi, nei popolamenti più vecchi e di età uniforme, possono crescere più rapidamente, questi popolamenti hanno un numero inferiore di alberi. La dinamica della popolazione arborea, in particolare la mortalità, può quindi contribuire in modo significativo al calo della produttività a livello di popolamento forestale23.
Per un'ampia maggioranza di specie, i nostri risultati supportano la previsione qualitativa della teoria dello "scaling metabolico", di una crescita in continuo aumento alla scala dei singoli alberi6, con diverse implicazioni. Ad esempio, la teoria della life-history spesso ipotizza che i compromessi tra crescita e riproduzione delle piante siano sostanziali11. Contrariamente ad alcune aspettative11,16, i nostri risultati indicano che per la maggior parte delle specie arboree i cambiamenti nell'allocazione riproduttiva, legati alle dimensioni, sono insufficienti a determinare diminuzioni a lungo termine dei tassi di crescita6. Inoltre, il calo della crescita è talvolta considerato una caratteristica distintiva della senescenza delle piante12. I nostri risultati sono quindi importanti per comprendere la natura e la prevalenza della senescenza nella storia della vita delle piante secolari27.
Infine, i nostri risultati sono rilevanti per la comprensione e la previsione dei feedback delle foreste al ciclo del carbonio terrestre e al sistema climatico globale1-3. Questi feedback saranno influenzati dagli effetti dei cambiamenti climatici, di uso del suolo e di altri fattori ambientali sui tassi di crescita e sulla struttura dimensionale delle popolazioni arboree, effetti che si stanno già osservando nelle foreste28,29. La rapida crescita dei grandi alberi indica che, rispetto al loro numero, potrebbero svolgere un ruolo estremamente importante in queste retroazioni30. Ad esempio, nelle foreste vetuste degli Stati Uniti occidentali, gli alberi con un diametro >100 cm costituiscono il 6% degli alberi, ma contribuiscono al 33% della crescita annuale della massa forestale. I modelli meccanicistici del ciclo del carbonio nelle foreste, dipenderanno da un'accurata rappresentazione della produttività su diverse scale di organizzazione biologica, compresa la calibrazione e la convalida, in relazione ad un accumulo di carbonio in continuo aumento a livello di singoli alberi.
Riferimenti
1. Pan, Y. et al. A large and persistent carbon sink in the world’sforests. Science n. 333, 2011, pp. 988–993.
2. Medvigy, D., Wofsy, S. C., Munger, J. W., Hollinger, D. Y. & Moorcroft, P. R., Mechanistic scaling of ecosystemfunction and dynamics in space and time:EcosystemDemography model version 2. Geophys. Res. n. 114, 2009, G01002.
3. Caspersen, J. P., Vanderwel, M. C., Cole, W. G. & Purves, D. W., How stand productivity results from size- and competition-dependent growth and mortality. PLoS ONE n. 6, 2011, e 28660,.
4. Kutsch, W. L. et al. in Old-GrowthForests: Function, Fate and Value, (a cura di) Wirth, C., Gleixner, G. & Heimann, M., Springer, 2009, pp. 57–79.
5. Meinzer, F. C., Lachenbruch, B. & Dawson, T. E. (a cura di), Size - and Age- Related Changes in Tree Structure and Function, Springer, 2011.
6. Enquist, B. J., West, G. B., Charnov, E. L. & Brown, J. H., Allometric scaling ofproduction and life-history variation in vascularplants, Nature, n. 401, p. 199, pp. 907–911.
7. Sillett, S. C. et al., Increasingwood production throughold age in tall trees, Ecol.Manage. n. 259, 2010, pp. 976–994.
8. Mencuccini, M. et al., Size-mediated ageing reduces vigour in trees, Ecol. Lett. n. 8, 2005, pp. 1183–1190.
9. Drake, J. E., Raetz, L. M., Davis, S. C. & De Lucia, E. H., Hydraulic limitation not declining nitrogen availability causes the age-related photosynthetic decline in loblolly pine (Pinus taeda L.), Plant Cell Environ., n. 33, 2010, pp. 1756–1766.
10. Ryan, M. G., Binkley, D. & Fownes, J. H., Age-related decline in forest productivity: pattern and process. Ecol. Res. n.27, 1997, pp. 213–262.
11. Thomas, S. C. in, Size- and Age-Related Changes in Tree Structure and Function (a cura di), Meinzer, F. C., Lachenbruch, B. & Dawson, T. E. Springer, 2011, pp. 33–64.
12. Thomas, H., Senescence, ageing and death of the whole plant. New Phytol. n. 197,2013, pp. 696–711.
13. Carey, E. V., Sala, A., Keane, R. & Callaway, R. M., Are old forest sunderestimated as global carbon sinks?, Change Biol. n. 7, 2001, pp. 339–344.
14. Phillips, N. G., Buckley, T. N. & Tissue, D. T., Capacity of old trees to respond to environmental change. Integr. Plant Biol. n. 50, 2008, pp. 1355–1364.
15. Piper, F. I. & Fajardo, A., No evidence of carbon limitation with tree age and height in Nothofagus pumilio under Mediterranean and temperate climate conditions. Bot. n.108, 2011, pp. 907–917.
16. Weiner, J. & Thomas, S. C., The nature of tree growth and the ‘‘age-related decline in forest productivity’’. Oikos n. 94, 2001, pp. 374–376.
17. Jenkins, J. C., Chojnacky, D. C., Heath, L. S. & Birdsey, R. A., Comprehensive Database of Diameter-based Biomass Regressions for North American Tree Species General Technical Report, NE-319, http://www.nrs.fs.fed.us/pubs/6725, USDA Forest Service, Northeastern Research Station, 2004.
18. Niklas, K. J. & Enquist, B. J., Canonical rules for plant organ biomass partitioning and annual allocation. J. Bot. n. 89, 2002, pp. 812–819.
19. Thomas, S. C., Photosynthetic capacity peaks at intermediate size in temperate deciduous trees. Tree Physiol. n. 30, 2010, pp. 555–573.
20. Steppe, K., Niinemets, Ü. & Teskey, R. O., in Size- and Age-Related Changes in Tree Structure and Function (a cura di), Meinzer, F. C., Lachenbruch, B. & Dawson, T. E., Springer, 2011, pp. 235–253.
21. Gilmore, D. W. & Seymour, R. S., Alternative measures of stem growth efficiency applied to Abies balsamea from fourcanopy positions in central Maine, USA. Ecol. Manage, n. 84, 1996, pp. 209–218.
22. Kaufmann, M. R. & Ryan, M. G., Physiographic, stand, and environmental effects on individual tree growth and growt hefficiency in subalpine forests. Tree Physiol. n. 2, 1986, pp. 47–59.
23. Coomes, D. A., Holdaway, R. J., Kobe, R. K., Lines, E. R. & Allen, R. B., A general integrative framework for modelling woody biomass production and carbon sequestration rates in forests. Ecol., n. 100, 2012, pp. 42–64.
24. Binkley, D. A., hypothesis about the interaction of tree dominance and stand production through stand development. Ecol. Manage, n. 190, 2004, pp. 265–271.
25. Pretzsch, H. & Biber, P., A re-evaluation of Reineke’s rule and stand density index. Sci., n. 51, 2005, pp. 304–320.
26. Kashian, D. M., Turner, M. G., Romme, W. H. & Lorimer, C. G., Variability and convergence in stand structural development on a fire-dominated subalpine landscape. Ecology, n. 86, 2005, pp. 643–654.
27. Munne´-Bosch, S., Do perennials really senesce? Trends Plant Sci., p. 13,2008, pp. 216–220.
28. Jump, A. S., Hunt, J. M. & Peñuelas, J., Rapid climate change-related growth decline at the southern range edge of Fagus sylvatica, ChangeBiol., n. 12, 2006, pp. 2163–2174.
29. Lindenmayer, D. B., Laurance, W. F. & Franklin, J. F., Global decline in large old trees. Science, n. 338, pp. 1305–1306.
30. Enquist, B. J., West, G. B. & Brown, J. H., Extensions and evaluations of a general quantitative theory of forest structure and dynamics. NatlAcad. Sci. USA n. 106, 2009, pp. 7046–7051.
N.L. Stephenson, et al.
Traduzione e revisione a cura della Redazione
Per l’accesso al testo originale dell’articolo, con metodi d’analisi e informazioni aggiuntive, non presenti nella traduzione: CLICCA QUI



Ai lettori-traduttori-editori che ci leggono l'invito a tradurlo.